|
Қатерлі ісікті емдеуге қатысты екі жаңалық
|
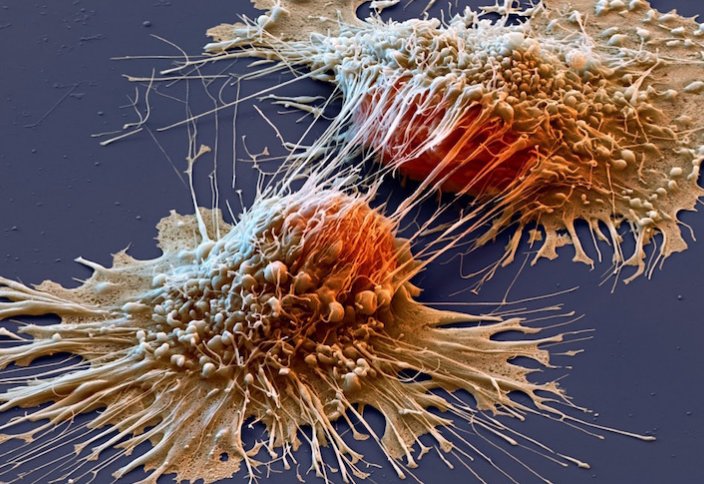
Қатерлі ісіктің бетін қайтарудың тың тәсілі табылды
Қатерлі ісікті емдеудің тың терапиясы оның жасушаларын ұйқы режиміне ауыстыруға негізделген. Осылайша обырдың рецидивіне (жазылғандай болып көрінген аурудың қайталануы) жол бермейді. Бұл жайында islam.kz порталы EurekAlert ақпарат көзіне сілтеме жасай отырып мәлім етеді. Қатерлі ісік рецидиві бір жылдан кейін немесе ондаған жылдардан кейін орын алуы мүмкін. Яғни, қатерлі ісіктің сылып тастаған соң аталған дерттің кез келген уақытта қайта пайда болуы ықтималдылығы жоғары. Мұның себебі – қатерлі ісіктің жекелеген жасушаларында жатыр, ұзақ уақыт бойы белгі бермей келеді де аяқ астынан көбейеді. Америкалық ғалымдар ұйқыдағы жасушаның оянуына жол бермейтін маңызды жаңалық ашуға қол жеткізе алды. Бұл арада NR2F1 ақуызы турасында сөз болып отыр – жасушалардың ұйқы режимінде қалуы аталған ақуызға байланысты – бұл ақуыз қатерлі ісік жасушасының ядросына еніп, белсенділікті оятатын генді іске қосады немесе ажыратады. Әдетте NR2F1 ақуызының деңгейі алғашқы ісік ошағында төмен болып келеді, алайда, ұйқы режиміндегі қатерлі ісік жасушаларында молынан кездеседі. Қатерлі ісік рецидиві NR2F1 ақуызының мөлшері азайғанда орын алады. Ғалымдар NR2F1 деңгейін арттыру арқылы қажетті терапевтік нәтижеге қол жеткізіп отыр - NR2F1 ақуызын белсендіретін C26 молекуласын тапты. Ғалымдар бұл тарапта C26 молекуласымен адам жасушасын өңдей отырып, NR2F1 ақуызының деңгейін арттырып, қатерлі ісіктің бетін қайтара алған.
Қатерлі ісікті цитокинді нанобөлшектермен жою тәсілі
Алдымене цитокин не екеніне аз-кем тоқтала кетпекпіз: цитокин – гормон тәріздес ақуыздар мен пептидтер тобы; иммундық жүйе жасушаларымен синтезделеді әрі секреттеледі; цитокиннің молекулярлық массасы (салмағы) 30 кДа-н аспайды. Бұл жайында islam.kz порталы lenta.ru ақпарат көзіне сілтеме жасай отырып мәлім етеді. Ресей ғалымдары қатерлі ісікті жоятын полимерлі нанобөлшектер ойлап тапты. Бұл нанобөлшектер жасушаның жойылуына апарып соқтыратын ісікке қарсыTRAIL DR5 ақуызымен байланысқан. TRAIL цитокині жасушаның бес рецепторымен өзара әрекеттеседі. Бұл бес рецептордың екеуі - DR4 және DR5 апоптоз сигналын тудырады, яғни, жасущаның жойылуын белгілейді, ал қалған үш рецептор сигналдың берілуін тежейді немесе мүлдем бұғаттап тастайды. Бұдан бөлек, организмнің өзі ісікітің бетін қайратарындай деңгейде цитокин істеп шығара алмайды, ал жасанды жолмен TRAIL цитокині осы олқылықтың орнын толтыра алады. Осылайша ғалымдар DR4 және DR5 рецепторларымен байланысу ықтималдылығы жоғары модификацияланған цитокин жасады. TRAIL DR5 модификацияланған цитокин организмдегі діттеген жерге амфифилдік (гидрофилді (ылғалдан қашпайтын) және гидрофобты (ылғалдан қашатын) ерекшеліктерге ие) полимерден тұратын нанобөлшектермен жеткізіледі. Су ерітіндісінде полимер молекуласы беткі жағы гидрофилді, ал ядросы гидрофобты болып келетін наномөлшердегі бөлшектерді өздігінен қалыптастырады. Бұл бөлшектер молекуланы өз ішіне енгізеді немесе молекуланы беткі жағымен алып жүреді. Әрбір бөлшектің көлемі шамамен 200 нанометрге дейін жетеді, ал бөлшектің өзі қатерлі ісікке қарсы TRAIL DR5-B цитокинінің бірнеше молекуласын қамти алады.