Прием псилоцибина связан со снижением творческих способностей. У людей резко уменьшается число новых идей и способность оценить их. Эффект сохраняется в течение недели после употребления вещества. При этом усиливается субъективное чувство спонтанной креативности и озарения. Об этом пишет N+1.
В исследовании голландских ученых из Маастрихтского университета участвовало 60 здоровых добровольцев. Все они когда-либо принимали психоделики, но не за три месяца до экспериментов.
Участников случайно разделили на две группы. Одна получала 0,17 мг/кг псилоцибина, а вторая — плацебо. Все добровольцы периодически заполняли опросник измененных состояний, также они выполнили два творческих задания. Результаты оценили независимые эксперты, которые не знали условий эксперимента.
Оказалось, что псилоцибин усиливает субъективное ощущение высокого качества генерируемых идей, несмотря на что объективных доказательств этому нет. То есть под действием психоделика люди переживали спонтанное творческое озарение, практически безосновательно считая свои идеи новыми и оригинальными.
При этом прием псилоцибина был связан с объективным ухудшением креативных способностей. Такое противоречие может говорить о том, что употребление психоделика, возможно, уменьшает потенциал преднамеренного творческого познания, резко увеличивая потенциал спонтанного творческого мышления
Исследователи научились управлять гидрогелем для доставки противораковых препаратов
Гидрогели состоят из скрепленных в единую сеть полимеров, между которыми находится вода. Эти материалы считаются перспективными контейнерами для доставки лекарственных средств благодаря тому, что они дешевы в изготовлении (относительно, например, липосом), биосовместимы и способны надежно сохранять лекарственные средства на протяжении всего их пути до опухоли.
Их можно ввести через шприц, а затем активировать в организме, например, инфракрасным светом. Также можно дать гидрогелям возможность реагировать на определенные стимулы в микроокружении опухоли, такие как набухание или сжатие при воздействии температуры или изменения рН. В ответ на эти стимулы гидрогели будут высвобождать лекарственные средства только в месте опухоли, не нанося вред здоровым тканям.
До сих пор разрабатываемые для этой цели гидрогели реагировали на один конкретный стимул, но японские ученые решили разработать более универсальное решение. Они создали материал из синтетических полимеров и органических соединений с включениями аминогрупп. Новый гидрогель может сжиматься и набухать в ответ как на изменение температуры, так и на изменение рН, и в результате высвобождать содержащиеся в нем лекарства.
Исследователи продемонстрировали это свойство в лабораторных экспериментах, в которых воспроизводили кислотность и температуру микроокружения опухоли. Сетчатая структура гидрогеля позволила сохранять лекарства в целости, пока не наступит момент для их высвобождения. Изменяя размер полимреной сетки, ученые смогли контролировать количество и тип доставляемого в организм препарата.
Статья об открытии опубликована в Journal of Controlled Release.
Ученые создали уникальную ткань для перевязки ран и повреждений
"Так называемая искусственная кожа, защищает больное место от механических повреждений и вредоносных инфекций, а также создает оптимальные условия для роста клеток, пропускает воздух и водные пары, чтобы рана под таким покрытием не высыхала и не мокла", - следует из релиза.
Ткань представляет собой тончайшую пленку, которая накладывается на раны, клетки ткани начинают переходить в рану, смешиваясь с клетками пациента, и активизируют выработку коллагена для зарастания раны и образования рубца, утверждают в пресс-службе.
Отмечается, что помимо лечения, ткань помогает защитить рану от внешних воздействий и избавит пациентов от бесконечных перевязок благодаря латексной подложке, которая после завершения лечения просто отсоединяется.
"Ежегодно учеными наукограда регистрируются десятки новых технологий, разработок и открытий в области биологии, химии, физики, фармацевтики и других наук, находящихся на их пересечении", - пояснила министр инвестиций, промышленности и науки Московской области Екатерина Зиновьева, слова которой приводятся в сообщении.
Ученые разработали антибактериальную гелевую повязку из шелухи дуриана
Ученые-диетологи из Технологического университета Наньян в Сингапуре (NTU Singapore) создали антибактериальный гелевый бинт, используя шелуху популярного тропического фрукта — дуриана.
Известный как «король фруктов» в Юго-Восточной Азии, дуриан имеет толстую шелуху с колючими шипами. Обычно ее выбрасывают. Однако ученые из NTU создали мягкий гель, похожий на листы кремния. Его можно разрезать на бинты различной формы и размеры. Исследователи извлекли высококачественную целлюлозу из шелухи дуриана и объединили ее с глицерином — побочным продуктом производства биодизеля и мыла.
Затем они добавили органические молекулы, полученные из пекарских дрожжей — натуральные дрожжевые фенолы. Этот компонент наделил повязку антибактериальными свойствами.
Детали работы опубликованы в рецензируемом журнале Американского химического общества ACS Sustainable Chemistry & Engineering.

Разные размеры гидрогелевых пластырей, полученных из дуриана, которые могут быть увеличены для хирургических ран или уменьшены для типичного размера повязки. Предоставлено: Наньянский технологический университет.
В аптеках широко доступны гидрогелевые пластыри, которые обычно используются для закрытия хирургических ран, чтобы свести к минимуму образование избыточной рубцовой ткани, что приводит к более мягкому и плоскому рубцу. При использовании обычных пластырей или марлевых повязок пластырь сохраняет кожу увлажненной, а не высыхает.
Проблема в том, что обычные гидрогелевые пластыри, представленные на рынке, изготавливаются из синтетических материалов — речь идет о таких полимерах, как как полиметакрилат и поливинилпирролидон. Ионы серебра или меди используются для придания повязкам антибактериальных свойств. Такие синтетические материалы, одобренные для использования в биомедицине, более дороги по сравнению с новым гидрогелем, изготовленным из природных отходов.
С растущей угрозой появления супербактерий, устойчивых к антибиотикам, миру потребуется множество альтернативных способов предотвращения инфекций, отмечают авторы исследования.
Кроме того, органическая гелевая повязка нетоксична и поддается биологическому разложению. А значит, она окажет меньшее воздействие на окружающую среду, чем обычные синтетические повязки.
Самособирающиеся нановолокна защищают повреждения от воспалений
Биоинженеры разработали самособирающийся наноматериал, который ограничит ущерб от воспалительных заболеваний путем активации ключевых клеток иммунной системы.
Одним из признаков воспалительных заболеваний, таких как ревматоидный артрит, болезнь Крона и псориаз, является избыточное производство сигнальных белков — цитокинов, вызывающих воспаление. Одним из наиболее значимых воспалительных цитокинов является белок TNF. Сейчас наилучшее лечение таких заболеваний включает использование искусственных антител — моноклональных антител. Их задача — нацеливаться на TNF и уничтожать их, уменьшая воспаление.
Хотя моноклональные антитела помогают лечить воспалительные заболевания, терапия не лишена недостатков. Проблема в высокой стоимости, а еще пациентам приходится регулярно делать себе инъекции. Кроме того, терапия отличается неравномерной эффективностью. Не стоит забывать и о том, что организм учится вырабатывать антитела, которые могут разрушить изготовленное лекарство.
Аспиранты лаборатории Collier придумали, как решить проблему с помощью новых наноматериалов. Они могут собираться в длинные нановолокна со специальным белком C3dg. Волокнам удалось активировать B-клетки иммунной системы для выработки антител и взаимодействии между различными клетками иммунной системы.
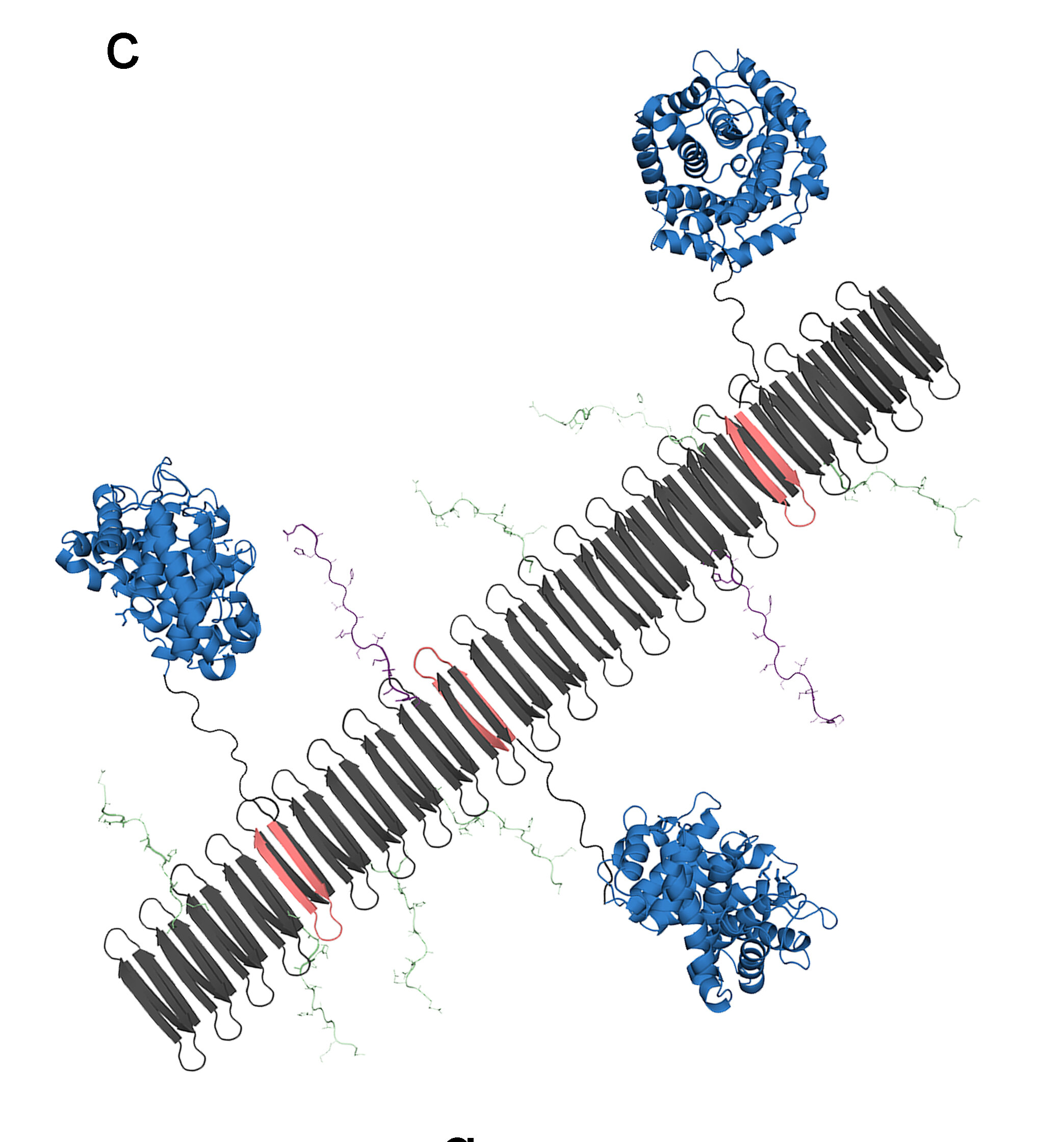
На графике показаны пептидные нановолокна, несущие белок комплемента C3dg (синий) и ключевые компоненты белка TNF, которые включают эпитопы B-клеток (зеленый цвет) и эпитопы T-клеток (фиолетовый цвет). Предоставлено: Челси Фрис, Университет Дьюка.
Ученые соединили ключевые фрагменты белка C3dg с компонентами TNF в нановолокна.
Когда команда проверила наноматериал на модели псориаза на мышах, то обнаружили, что нановолокна с белком C3dg столь же эффективны, как и терапия моноклональными антителами. И, поскольку C3dg и так находится в организме, антитела его не атакуют.
Изучив модель псориаза, ученые сделали удивительное открытие — C3dg не только стимулировал выработку антител в B-клетках, но и повлиял на реакцию T-клеток. В дальнейшем исследователи надеются продолжить изучение механизмов, которые лежат в основе полезной активации Т-клеток.
Микроимплант в реальном времени измеряет уровень кислорода в тканях глубоко под кожей
Беспроводной имплант, разработанный инженерами Калифорнийского университета в Беркли, измеряет насыщение кислородом живых тканей глубоко под поверхностью кожи.
Устройство, которое по размеру меньше средней божьей коровки и питается от ультразвуковых волн, поможет врачам контролировать состояние пересаженных органов или тканей. Таким образом оно обеспечит раннее предупреждение о потенциальных проблемах после трансплантации.
Кроме того, технология открывает путь для создания множества миниатюрных датчиков. Они смогут отслеживать другие ключевые биохимические маркеры в организме, такие как pH или углекислый газ. Однажды они предоставят врачам минимально инвазивные методы мониторинга биохимии внутри функционирующих органов и тканей.
Используя ультразвуковую технологию в сочетании с интегральной схемой, можно создавать сложные имплантаты, которые проникают очень глубоко в ткани для получения данных от органов, отмечают ученые.
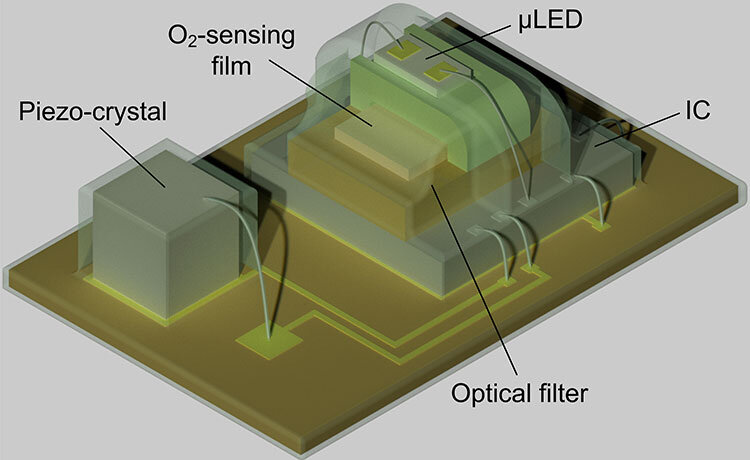
Схема кислородного имплантата размером 4,5 см в длину и 3 см в ширину. ΜLED, O2-чувствительная пленка и оптический фильтр составляют кислородный датчик и управляются интегральной схемой (IC). Пьезокристалл преобразует электронный сигнал от ИС в ультразвуковые волны, которые могут безопасно передаваться через живые ткани. Предоставлено: Калифорнийский университет в Беркли, изображение Сонера Сонмезоглу.
Большинство методов измерения оксигенации тканей предоставляют информацию только о том, что происходит у поверхности тела. Они основаны на электромагнитных волнах, которые проникают только на несколько сантиметров под кожу или ткани органа. Хотя существуют типы магнитно-резонансной томографии, которые предоставляют информацию о насыщении кислородом глубоких тканей, они занимают много времени и не предоставляют данные в режиме реального времени.
Новый датчик отличается от пульсоксиметров, которые используются для оценки насыщения крови кислородом. В то время как они измеряют долю гемоглобина в крови, устройство напрямую измеряет количество кислорода в тканях.
Имплантат размером 4,5 см в длину и 3 см в ширину состоит из ΜLED, O2-чувствительной пленки и оптического фильтра. Само устройство управляются интегральной схемой (IC). Пьезокристалл преобразует электронный сигнал от IC в ультразвуковые волны, которые безопасно передаются через живые ткани.
Одно из возможных применений датчика — мониторинг пересаженных органов. Дело в том, что через несколько месяцев после трансплантации могут возникнуть сосудистые осложнения, которые приводят к дисфункции трансплантата.
Ученые продемонстрировали «врастающий» под кожу датчик состава крови
Новый инструмент использует модифицированные наночастицы из золота, погруженные в биосовместимый гидрогель, в который прорастают живые капилляры.
В последние годы ученые разных стран активно работают над созданием миниатюрных датчиков, которые были бы способны отслеживать содержание в крови различных веществ. Важно, чтобы при этом прибор функционировал незаметно и комфортно для пациента, не вызывал отторжения организмом и не требовал регулярного вмешательства для замены батареек или реактивов. Действующий прототип такого устройства продемонстрировали недавно разработчики из Университета Гутенберга (JGU) в немецком Майнце.
Датчик использует цветные золотые наночастицы, связанные со специфическими рецепторами для целевых веществ и погруженные в инертный полимер. По словам профессора JGU Карстена Зонихсена (Carsten Sönnichsen), готовое устройство «словно невидимая татуировка размерами не больше монеты и тоньше миллиметра» и уже успешно испытано при имплантации под кожу лабораторных животных. Об этом Зонихсен с коллегами пишут в статье, опубликованной в журнале Nano Letters.
Наночастицы золота способны сильно поглощать и рассеивать инфракрасное излучение. Эту их способность ученые активно пытаются применить для лечения, диагностики и науки. Команда профессора Зонихсена дополнила такие наночастицы молекулами, способными связывать то или иное нужное вещество (в проведенных экспериментах — антибиотик канамицин). Его появление меняет окружение наночастиц, влияя на длину рассеянного света, что можно зарегистрировать с помощью внешних датчиков, сквозь кожу.
Модифицированные наночастицы помещаются в биосовместимый гидрогель — пористый, заполненный жидкостью полимер, который не вызывает иммунного ответа. После имплантации под кожу в гидрогель прорастают тончайшие капилляры, которые и приносят целевое вещество к наночастицам. В экспериментах с безволосыми лабораторными крысами было показано, что датчик позволяет регистрировать присутствие разных доз канамицина в крови и стабильно работает на протяжении как минимум нескольких месяцев.

Сверточные нейронные сети обучили брать кровь на анализ быстро и безболезненно
Исследователи из Сколковского института науки и технологий (Сколтех) разработали первый прототип медицинской системы визуализации. Она позволит точнее и менее болезненно брать кровь у пациетов на анализ.
Новая разработка Сколтеха основана на использовании нейронных сетей для анализа изображений вен в ближнем ИК-диапазоне и проецирования рисунка вен прямо на тело пациента. Новый метод поможет упростить забор венозной крови и снизить ощущения дискомфорта у пациентов. Особенно обновенный процесс забора крови будет полезен людям с диабетом.
Подробности исследования опубликованы в сборнике трудов XVI Международной конференции по управлению, автоматизации, робототехнике и техническому зрению (ICARCV).
Ежедневно в мире выполняется около 20 миллионов анализов крови. Авторы статьи приводят данные, согласно которым в 45% случаев забор крови вызывает определенный дискомфорт у пациентов в силу различных причин, затрудняющих доступ к венам. Если вены плохо видны и не пальпируются, возникает риск травматизации при заборе крови. Также множественные или неточные проколы приводят к риску возникновения тахикардии.
Доцент Центра Сколтеха по научным и инженерным вычислительным технологиям для задач с большими массивами данных (CDISE), руководитель группы вычислительной визуализации Сколтеха Дмитрий Дылов и его коллеги разработали интеллектуальный сканер вен ближнего ИК-диапазона. Он позволяет достаточно точно определять контуры вен на ногах и руках. Стоит отметить, что делать это можно в полностью автоматическом режиме без использования каких-либо пользовательских данных.
«Инфракрасные сканеры вен уже широко применяются в клинической практике, однако наш прибор является первой разработкой, основанной целиком и полностью на передовых методах искусственного интеллекта. Одна нейронная сеть отвечает за шумоподавление и обработку инфракрасного сигнала, вторая определяет контуры вен, а третья постоянно следит за тем, чтобы вычисленные очертания сосудов совпадали с их фактическими границами», — объясняет Дылов.
Нейронная сеть — математическая модель, а также ее программное или аппаратное воплощение, построенная по принципу организации и функционирования биологических нейронных сетей — сетей нервных клеток живого организма. В свою очередь, сверточные нейронные сети нацелены на эффективное распознавание образов, которое входит в состав технологий глубокого обучения. Использует некоторые особенности зрительной коры, в которой были открыты так называемые простые клетки, реагирующие на прямые линии под разными углами, и сложные клетки, реакция которых связана с активацией определенного набора простых клеток. Таким образом, идея сверточных нейронных сетей заключается в чередовании свёрточных и субдискретизирующих слоев. Структура сети — однонаправленная (без обратных связей), принципиально многослойная. Для обучения используются стандартные методы, чаще всего метод обратного распространения ошибки. Функция активации нейронов (передаточная функция) — любая, по выбору исследователя.
В новой работе ученые адаптировали нейросети для создания системы, которая находит кровеносные сосуды пациента.
На этапе обучения специалисты объяснили системе, «что такое хорошо и что такое плохо». Все остальное нейронные сети сделали сами: автоматически нашли оптимальные настройки для новых пациентов, определили внешние условия и даже отследили искажения, в том числе и те, с которыми система ранее не сталкивалась.
Ученые проверили работу этой системы на наборе снимков рук пациентов, а после создали прототип устройства и проверили на добровольцах.
Авторы разработки отмечают, что сканер может масштабироваться для использования на других частях тела, а также применяться в ветеринарных клиниках для выполнения сложных проколов вен у животных.
Ученые работают над созданием "лазера из крови"
Американские ученые работают над созданием "лазера из крови", который будет излучать инфракрасный свет, сообщает "Вести.Ru" со ссылкой на публикацию в научном журнале Optica. Предполагается, что такой лазер позволит врачам отслеживать раковые опухоли.
Специалисты уверяют, что лазеры могут быть сделаны из различных материалов, включая живые клетки или желе. При создании лазера необходим источник света, материал, который его усилит, и отражающий резонатор. Сюйдун Фань (Xudong Fan) и его коллеги из Мичиганского университета использовали специальный краситель для своего кровяного лазера. Краситель светится в ближнем инфракрасном свете, и его же, кстати, вводят в кровь для использования при медицинском сканировании. По словам Фаня, сияние станет гораздо ярче, если его превратить в лазер.
Исследователи обнаружили, что краситель светится при смешивании с белками плазмы крови, тем самым повышая свою способность усиливать свет. Он накапливается в кровеносных сосудах, поэтому тела с большим количеством сосудов, такие как опухоли, должны светиться гораздо ярче, говорит ученый.
Теперь исследователям необходимо протестировать лазер на тканях животного, а это значит, что нужно придумать способ ввести в тело отражающий резонатор. Ученые считают, что в этом помогут наночастицы золота.














