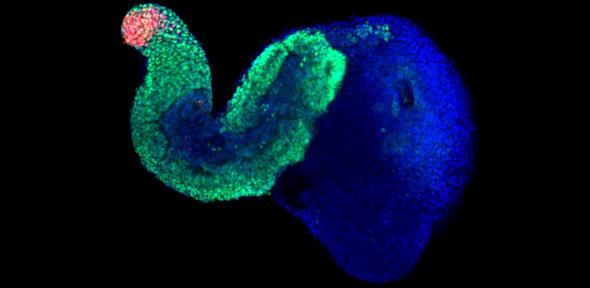
Эмбриологи создали из клеток кожи первую модель эмбриона человека на ранней стадии развития. Это позволит обойти запрет на такого рода опыты в большинстве стран. Рассказываем, можно ли считать зародышем такой организм, как его создали и чем он поможет науке.
О каких эмбрионах идет речь?
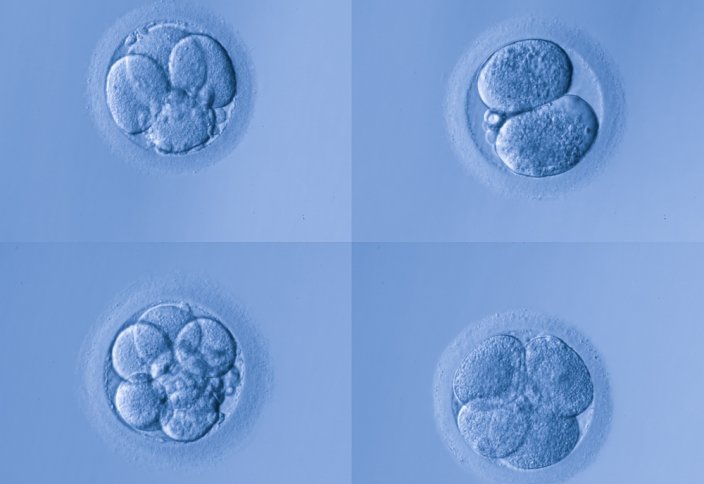
О бластоцисте. Это ранняя стадия развития зародыша млекопитающих (в том числе человека). Стадия бластоцисты следует за стадией морулы и предшествует стадии зародышевого диска. Стадия бластоцисты относится к преимплантационному периоду развития, то есть самому раннему периоду эмбриогенеза млекопитающих (до прикрепления зародыша к стенке матки).
В эволюции млекопитающих бластоциста как стадия развития возникла для обеспечения имплантации, а также для организации пространственной основы формирования зародышевого диска при отсутствии желтка.
Стадия бластоцисты не гомологична стадии бластулы. Стадия бластулы следует в онтогенезе млекопитающих позже (зародышевый диск), в т. н. «первую фазу гаструляции», но традиционно термин «бластула» к млекопитающим и другим амниотам не применяют. Соответственно распространенной ошибкой является употребление слова «бластоцель» по отношению к полости бластоцисты.
Внешне бластоциста представляет собой шар, состоящий из нескольких десятков или сотен клеток. Размер бластоцисты колеблется от долей миллиметра (0,1 мм у грызунов и человека) до нескольких миллиметров (у непарнокопытных).
Бластоциста состоит из двух клеточных популяций: трофобласта (трофэктодермы) и эмбриобласта (внутренней клеточной массы). Трофобласт формирует внешний слой эмбриона — полый шар или пузырек.
Эмбриобласт формирует внутренний слой бластоцисты, располагается внутри трофобластатического пузырька в виде скопления клеток у одного из полюсов шара (внутренняя клеточная масса).
Трофобласт участвует в имплантации (прикрепление эмбриона к эпителию матки, инвазия внутрь эндометрия матки, иммуносупрессорное действие, разрушение кровеносных сосудов), а также в формировании эктодермы ворсинок хориона (эктодермальная часть плаценты).
Эмбриобласт дает начало собственно телу плода, а также мезодермальным и энтодермальным структурам внезародышевых органов (желточному мешку, аллантоису, амниону, мезодермальной части хориона).
Партеногенез
Обычно эмбрионы в лабораторных условиях выращивают из донорских оплодотворенных яйцеклеток. В случае клонирования от сперматозоидов можно отказаться.
Начиная с середины десятых годов стало понятно, что вырастить зародыши в пробирке можно без участия половых клеток вообще. Бластоциста состоит из трех типов клеток, из которых потом формируются ткани плода, плацента и желточный мешок. А получают все это из стволовых клеток.
В начале 2000 гг. было показано, что обработкой in vitro ооцитов млекопитающих (крыс, макак, а затем и человека) либо предотвращением отделения второго полярного тельца при мейозе возможно индуцировать партеногенез, при этом в культуре развитие можно довести до стадии бластоцист.
Полученные таким образом бластоцисты человека потенциально являются источником плюрипотентных стволовых клеток, которые могут быть использованы в клеточной терапии.
В 2004 году в Японии слиянием двух гаплоидных ооцитов, взятых у разных особей мыши, удалось создать жизнеспособную диплоидную клетку, деление которой привело к формированию жизнеспособного эмбриона, который, пройдя стадию бластоцисты, развился в жизнеспособную взрослую особь.
Предполагается, что этот эксперимент подтверждает участие геномного импринтинга в гибели эмбрионов, образующихся из ооцитов, полученных от одной особи, на бластоцистарной стадии.
Беременность стволовыми клетками
Исследователи из Утрехтского университета создали мышиный эмбрион из стволовых клеток двух типов — эмбриональных и трофобластных. У выращенной ими бластоцисты сформировались все типы клеток, необходимые для дальнейшего развития.
Более того, при имплантации в матку животного бластоциста вызывала беременность. Правда, авторы работы подчеркивали, что у них получился не совсем настоящий зародыш и потому самка не смогла бы его выносить и родить.
В 2019 году ученые из Института биологических исследований Солка также инициировали беременность у мышей, пересадив им эмбрионы, полученные всего из одной соматической клетки. Ее взяли из организма взрослого животного, перепрограммировали и размножили — таким образом появилась культура зародышевых стволовых клеток.
Затем их перепрограммировали еще раз, превратив в так называемые улучшенные плюропотентные клетки, и обработали коктейлем из специальных сигнальных веществ — тех, которые при естественном эмбриональном развитии вызывают дифференцировку трофобласта (из него формируется плацента) и внутренней клеточной массы (из нее образуются ткани зародыша).
В результате в 15% случаев из них вырастали бластоиды — структуры, аналогичные бластоцистам по клеточному составу и экспрессии генов.
Статус человеческого эмбриона
Вопрос о статусе человеческого эмбриона рассматривается, среди прочего, в рамках биоэтики. Ключевое значение при таком рассмотрении имеет признание или непризнание «человеческого» содержания у эмбриона.
На данный момент статус эмбриона в российском законодательстве не до конца ясен, поскольку трудно «ответить на вопрос о том, воспринимает ли право идею существования эмбриона как субъекта правоотношений».
В частности закон «О трансплантации органов и (или) тканей человека» рассматривает эмбрионы как разновидность человеческих органов, хотя его действие на эмбрионы не распространяется. Далее существует представление о невозможности считать эмбрион человеком, «так как он не обладает правоспособностью».
В то же время юридическая мысль признает, что к человеческим органам эмбрион отнесен быть не может, поскольку является новым организмом со своими собственными органами.
Осознается и тот факт, что «в эмбрионе заложены все основы жизни». Таким образом, ситуацию следует признать сложной в силу двойственности правовой природы эмбрионов, что создает серьезные правовые проблемы, ибо «возникает вопрос о том, может ли эмбрион быть объектом правоотношений».
- Право собственности на эмбрионы
Эмбрионы становятся предметом имущественных споров в разных странах, включая США. Весьма известно так называемое дело Дэвисов (слушалось в 1989 году в штате Теннеси), когда в процессе раздела имущества разводящихся супругов возник вопрос о правах на ранее замороженные эмбрионы.
В итоге суд передал эмбрионы матери во временное владение для целей имплантации. Кроме того, суд установил, что человеческая жизнь начинается с момента зачатия и что по этой причине эмбрион не является объектом права собственности.
Однако в другом деле, которое слушалось в Нью-Йорке в 1995 году, эмбрионы были переданы бывшей жене в собственность. Известен также случай, когда супруги требовали изъять из лаборатории ранее переданный ими на исследование эмбрион.
В итоге суд потребовал передать эмбрион супругам, не обнаружив, однако наличия права собственности и подтвердив, «что человеческий эмбрион не является объектом права собственности».
Таким образом, американская правовая мысль в принципе готова признать эмбрион объектом правоотношений, однако этот объект весьма специфичный: как правило, суды не признают право собственности на эмбрионы, поскольку последние являются началом новой человеческой жизни.
- Права эмбриона
В дискуссиях о приемлемости или неприемлемости тех или иных манипуляций с эмбрионами важное место занимает понятие прав эмбриона. В частности запрет на использование эмбриона или эмбриональных тканей в целях медицинских исследований основан на признании таких прав.
Их защитники, сторонники так называемой консервативной позиции, ссылаются на то, что с момента зачатия человеческая жизнь свята и неприкосновенна, а также утверждают, что эмбрион обладает всеми человеческими правами.
Сторонники так называемой либеральной позиции даже на самых поздних стадиях беременности отказываются признавать самостоятельный статус плода, а решение его судьбы отдается матери или медикам.
Естественные неотчуждаемые права человека включают, среди прочего, право на жизнь. Вопрос о том, каков момент возникновения права на жизнь, от которого и берет свой отсчет правосубъектность, крайне важен для уголовного и гражданского права и для юриспруденции в целом.
Существует представление, согласно которому правовой статус эмбриона должен определяться на основе того факта, что эмбрион является началом новой жизни, а не частью человеческого организма. Сторонники этой позиции исходят из того, что человек как новое существо (биологический индивидуум) возникает сразу после слияния родительских половых клеток.
Зачем выращивать эмбрионы?
Для того, чтобы обойти довольно суровые правила, напрямую запрещающие создавать зародыши человека в исследовательских целях. А без этого невозможно разобраться, что на самом деле происходит на ранних стадиях развития.
Вполне вероятно, что общество в целом будет относиться к исследованиям на таких моделях более терпимо, чем к опытам над настоящими эмбрионами, считают в редакционной статье Nature исследователи из Мичиганского университета (США). Пока главный этический вопрос, который стоит решить, — применимо ли к ним правило 14 дней.
Сегодня человеческие эмбрионы, полученные экспериментально, уничтожают через 14 дней после оплодотворения. В одних странах нарушение этой нормы карается законодательно, в других — опыты с подобными зародышами отклоняют этические комитеты и лишают финансирования.
Если же в отношении бластоидов запрет отменят, то ученым, вероятно, удастся разобраться не только с причинами выкидышей и неудачами при ЭКО, но и выяснить механизмы целого ряда наследственных патологий — в том числе сердечно-сосудистых заболеваний и некоторых типов диабета.
Человеческий эмбрион собрали из лабораторных клеток
Искусственный псевдозародыш, готовый прикрепиться к матке, может стать удачной моделью для изучения патологий эмбрионального развития.
Сразу две исследовательские группы, в Юго-западном медицинском центре Университета Техаса и в Университете Монаша, сообщили в Nature, что им удалось лабораторными методами создать полноценный человеческий эмбрион на стадии бластоцисты. Так называют одну из самых ранних стадий развития – на этапе бластоцисты эмбрион ещё не внедрился в стенку матки, но уже готов это сделать.
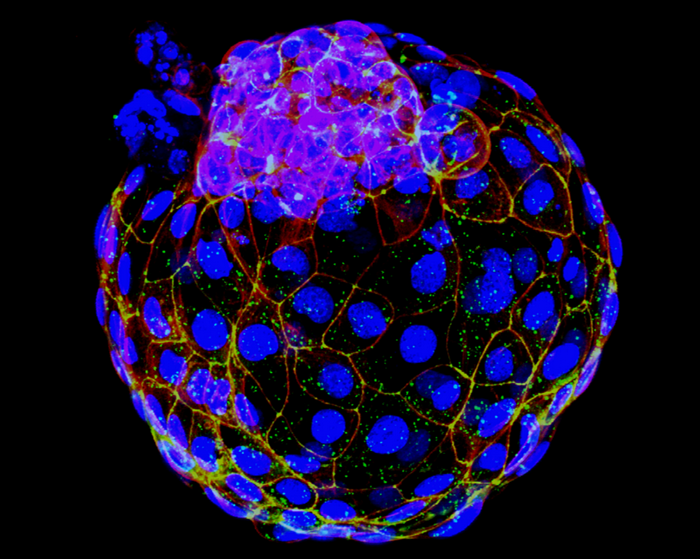
Что такое бластоциста? После оплодотворения яйцеклетка млекопитающих первые несколько дней делится, пока из неё не получится что-то вроде пузырька. В этом пузырьке есть клетки трёх типов. Те, что окружают его по периметру, образуют так называемый трофобласт, или трофэктодерму. Клетки трофобласта потом сформируют плаценту. Большая часть объёма внутри пузырька – просто полость, которая так и называется – полость бластоцисты. Но в одном месте изнутри на стенке пузырька образуется клеточная масса, которая опять же так и называется – внутренняя клеточная масса. Она состоит из эпибласта и гипобласта. Клетки гипобласта потом дадут зародышевый мешок, который помогает эмбриону питаться и дышать на самых ранних этапах развития, и хорион – ещё одну зародышевую оболочку, которая будет участвовать в формировании плаценты. А вот само тело эмбриона начнёт развиваться из клеток эпибласта.
По мере развития молекулярной и клеточной биологии исследователи стали пытаться смоделировать бластоцисту в лабораторных условиях. В этом есть смысл не только с точки зрения фундаментальных знаний о том, как развивается зародыш, но и из практических соображений: многие патологии развития и неудачные беременности начинаются с проблем на стадии бластоцисты. Несколько лет назад лабораторную бластоцисту удалось собрать из мышиных стволовых клеток – полученную клеточную структуру назвали бластоид, чтобы отличать от натуральной бластоцисты. И вот сейчас то же самое получилось с клетками человека.
Главная проблема была в том, чтобы найти стволовые клетки, похожие на клетки бластоцисты. Исследователи из Техасского университета брали их из двух источников. Во-первых, это были настоящие клетки человеческой бластоцисты. Когда-то человеческую бластоцисту взяли для научных исследований, разобрали на клетки, и с тех пор их сохраняют для экспериментов. (Клетки зародыша потенциально бессмертны, если их правильно содержать.)
Во-вторых, зародышевые клетки можно получить из обычных клеток взрослого человека – это будут так называемые индуцированные плюрипотентные стволовые клетки. Индуцированные – потому что их создают, обрабатывая обычные клетки специальными молекулярными сигналами. В результате, например, клетки кожи теряют специализацию и впадают в глубокое эмбриональное детство, когда они могли бесконечно делиться. Зародышевые клетки способны превратиться в любые другие, поэтому их называют плюрипотентными. Мы много раз писали про такие стволовые клетки; по свойствам они не отличаются или почти не отличаются от настоящих зародышевых клеток.
Исследователи выращивали клетки в специальном сосуде, который позволял им образовать трёхмерную структуру. То есть если бы стволовые клетки захотели создать бластоцисту (бластоид), им бы ничто не помешало. Разумеется, в питательную среду им добавляли молекулярные факторы, которые должны были склонить делящиеся клетки к тому, чтобы сформировать пузырёк с трофобластом, эпибластом и гипобластом.
Другая группа исследователей, в Университете Монаша, тоже работали со специализированными клетками взрослых людей. Но эти клетки не обращали в индуцированные стволовые, а добивались того, чтобы среди них сразу появились бластоцистные клетки трёх видов. То есть первая исследовательская команда «обнуляла» генетическую активность зрелых клеток до самого-самого начального зародышевого состояния, а потом запускала в них программу зародышевого развития – и делящиеся клетки уже сами превращались в клетки трофобласта, эпибласта и гипобласта. А вторая команда сразу пыталась получить клетки трофобласта, эпибласта и гипобласта, которые объединялись в псевдозародыш-бластоид. В первом случае бластоцисту выращивали, во втором – собирали из клеточного конструктора (точнее, детали конструктора сами находили себя и соединялись в нужную структуру).
И в том, и в другом случае всё сработало более-менее успешно: человеческие бластоиды формировались на 6–8 день выращивания клеточной культуры и с 20-процентным успехом. Размером и структурой они были как настоящие, состояли примерно из такого же числа клеток. Активность генов в искусственной бластоцисте тоже была такая же, как у настоящей, готовой имплантироваться в матку. Собственно, когда для полученных бластоидов имитировали условия имплантации, они были на это готовы: они прикреплялись к клеточной культуре, которая изображала стенку матки, и начинали развиваться дальше. У них появлялись зародышевые органы вплоть до того, что некоторые псевдоэмбрионы готовили свои клетки, чтобы создать плаценту.
То есть в принципе клеточные структуры, полученные подобным образом, вполне могут служить моделью для изучения человеческого зародыша в тот момент, когда он готовится укорениться в матке. Хотя портал Nature пишет о неизбежных этических вопросах, которые всегда возникают при слове «эмбрион», эти вопросы, очевидно, будут не столь остры, чем если бы речь шла о настоящем эмбрионе, полученном при слиянии яйцеклетки и сперматозоида. Правда, прежде чем на человеческих бластоидах начнут что-то изучать, нужно скорректировать методы, с помощью которых их получают.
Пока что псевдоэмбрионы, полученные так, как описано выше, развиваются с разной скоростью, и даже разные типы клеток в пределах одного и того же бластоида тоже могут развиваться с немного разной скоростью – хотя в настоящих зародышах всё строго синхронизировано. Наконец, в бластоидах оставалась группа клеток, которая не относится ни к трофобласту, ни к эпибласту, ни к гипобласту, и исследователям ещё предстоит понять, что это за клетки и как от них избавиться.